Вакцина
Для других целей см. раздел Вакцинация (неопределенность).
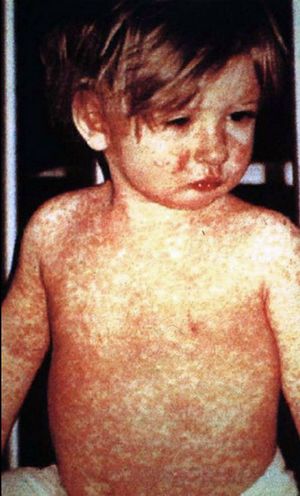
Вакцина-это биологический препарат, который обеспечивает активный приобретенный иммунитет к тому или иному инфекционному заболеванию . Вакцина обычно содержит агент, который напоминает болезнетворный микроорганизм и часто производится из ослабленных или убитых форм микроба, его токсинов или одного из его поверхностных белков. Агент стимулирует иммунную систему организма распознавать агент как угрозу, уничтожать его, а также дополнительно распознавать и уничтожать любые микроорганизмы, связанные с этим агентом, с которыми он может столкнуться в будущем. Вакцины могут быть профилактическими (чтобы предотвратить или улучшить последствия будущей инфекции естественным или" диким " патогеном), или терапевтический (чтобы бороться с болезнью, которая уже произошла, например, рак).
Введение вакцин называется вакцинацией . Вакцинация является наиболее эффективным методом профилактики инфекционных заболеваний; широко распространенный иммунитет , обусловленный вакцинацией , в значительной степени отвечает за искоренение оспы во всем мире и ограничение распространения таких заболеваний, как полиомиелит, корь и столбняк во многих странах мира. Эффективность вакцинации была широко изучена и проверена; например, вакцины, доказавшие свою эффективность, включают вакцину против гриппа , вакцину против ВПЧ и вакцину против ветрянки . Всемирная Организация Здравоохранения (ВОЗ) сообщает, что в настоящее время имеются лицензированные вакцины для 25 различных предотвратимых инфекций .
Термины вакцина и вакцинация происходят от Variolae vaccinae (оспа коровы), термин, разработанный Эдвардом Дженнером для обозначения коровьей оспы . Он использовал его в 1798 году в длинном названии своего исследования Variolae vaccinae, известного как коровья оспа , в котором он описал защитный эффект коровьей оспы против оспы . в 1881 году, чтобы почтить Дженнера, Луи Пастер предложил, чтобы эти термины были расширены, чтобы охватить новые защитные прививки, которые затем разрабатываются.
Вака - корова (латынь) .Тавр - бык.
Эффективность[править]
Существует подавляющее научное единодушие в отношении того, что вакцины являются весьма безопасным и эффективным способом борьбы с инфекционными заболеваниями и их искоренения. Тем не менее существуют ограничения на их эффективность. иногда защита терпит неудачу из-за неудачи, связанной с вакциной, такой как неудачи в ослаблении вакцины, режимах вакцинации или введении или неудачи, связанной с хозяином из-за иммунной системы хозяина просто не реагирует адекватно или вообще. Отсутствие ответа обычно является результатом генетики, иммунного статуса, возраста, состояния здоровья или питания. Он также может потерпеть неудачу по генетическим причинам, если иммунная система хозяина не включает штаммы в-клеток, которые могут генерировать антитела, пригодные для эффективного реагирования и связывания с антигенами, связанными с патогеном .
Даже если хозяин вырабатывает антитела, защита может быть неадекватной; иммунитет может развиваться слишком медленно, чтобы быть эффективным во времени, антитела не могут полностью отключить патоген, или может быть несколько штаммов патогена, не все из которых одинаково восприимчивы к иммунной реакции. Тем не менее, даже частичный, поздний или слабый иммунитет, такой как тот, который возникает в результате перекрестного иммунитета к штамму, отличному от целевого штамма , может смягчать инфекцию , приводя к более низкой смертности, более низкой заболеваемости и более быстрому выздоровлению.
Адъюванты обычно используются для усиления иммунного ответа, особенно для пожилых людей (50-75 лет и старше), у которых иммунный ответ на простую вакцину может быть ослаблен.
Эффективность или эффективность вакцины зависит от ряда факторов:
- само заболевание (при некоторых заболеваниях вакцинация проводится лучше, чем при других)
- штамм вакцины (некоторые вакцины специфичны или, по крайней мере, наиболее эффективны против конкретных штаммов заболевания)
- был ли правильно соблюден график вакцинации.
- своеобразный ответ на вакцинацию; некоторые люди являются "невосприимчивыми" к определенным вакцинам, что означает, что они не генерируют антитела даже после правильной вакцинации.
- различные факторы, такие как этническая принадлежность, возраст или генетическая предрасположенность.
Если привитое лицо действительно развивает заболевание, привитое против (прорывной инфекции), болезнь, вероятно, будет менее вирулентной, чем у невакцинированных жертв.
Ниже приведены важные соображения в отношении эффективности программы вакцинации:
- тщательное моделирование с целью прогнозирования воздействия кампании иммунизации на эпидемиологию заболевания в среднесрочной и долгосрочной перспективе
- постоянный эпиднадзор за соответствующим заболеванием после введения новой вакцины
- поддержание высоких показателей иммунизации, даже когда заболевание стало редким.
В 1958 году в Соединенных Штатах было зарегистрировано 763 094 случая заболевания корью, в результате чего 552 человека умерли. после введения новых вакцин число случаев заболевания снизилось до менее чем 150 в год (медиана 56). в начале 2008 года было зарегистрировано 64 предполагаемых случая заболевания корью. Пятьдесят четыре из этих инфекций были связаны с импортом из другой страны, хотя только 13% были фактически приобретены за пределами Соединенных Штатов; 63 из 64 человек либо никогда не прививались против кори, либо не были уверены, были ли они привиты.
Вакцинация привела к искоренению оспы-одного из самых заразных и смертельно опасных заболеваний человека.Другие болезни, такие как краснуха , полиомиелит, корь, свинка , ветряная оспа и брюшной тиф, уже не так распространены, как сто лет назад, благодаря широко распространенным программам вакцинации. До тех пор, пока подавляющее большинство людей вакцинировано, вспышка болезни происходит гораздо труднее, не говоря уже о распространении. Этот эффект называется стадным иммунитетом . Полиомиелит, который передается только между людьми, является мишенью обширной кампании по искоренению это привело к эндемическому полиомиелиту, ограниченному только частями трех стран (Афганистан , Нигерия и Пакистан ).[26] однако из-за трудностей, связанных с охватом всех детей, а также из-за культурных недоразумений предполагаемая дата ликвидации была несколько раз упущена.
Вакцины также помогают предотвратить развитие антибиотикорезистентности. Например, благодаря значительному снижению заболеваемости пневмонией, вызванной Streptococcus pneumoniae, программы вакцинации позволили значительно снизить распространенность инфекций, устойчивых к пенициллину или другим антибиотикам первой линии.
По оценкам, вакцина против кори способна предотвратить 1 миллион смертей в год.
Отрицательные последствия[править]
Вакцинация, проводимая в детском возрасте, в целом безопасна.[29] побочные эффекты, если таковые имеются, как правило, являются умеренными. частота побочных эффектов зависит от рассматриваемой вакцины. некоторые общие побочные эффекты включают лихорадку, боль вокруг места впрыски, и боли мышцы. Кроме того, у некоторых людей может быть аллергия на ингредиенты вакцины. вакцина MMR редко ассоциируется с фебрильными припадками .
Тяжелые побочные эффекты встречаются крайне редко. вакцина против ветряной оспы редко ассоциируется с осложнениями у иммунодефицитных лиц, а ротавирусные вакцины умеренно ассоциированы с инвагинацией .
По меньшей мере в 19 странах существуют программы компенсации "без вины", предусматривающие выплату компенсации тем, кто страдает от серьезных негативных последствий вакцинации. программа Соединенных Штатов известна как национальный закон о детской вакцине от травм, и Соединенное Королевство использует компенсацию ущерба от вакцины .
Типы[править]
Вакцины содержат мертвые или инактивированные организмы или очищенные продукты, полученные из них.
Существует несколько типов используемых вакцин.[33] они представляют собой различные стратегии, используемые для снижения риска заболевания при сохранении способности индуцировать благоприятный иммунный ответ.
Инактивированный[править]
Основная статья: Инактивированная вакцина
Некоторые вакцины содержат инактивированные, но ранее вирулентные микроорганизмы, которые были уничтожены химическими веществами, теплом или радиацией. примеры включают вакцину против полиомиелита , вакцину против гепатита А , вакцину против бешенства и некоторые вакцины против гриппа .
Ослабленный[править]
Основная статья: Аттенуированная вакцина
Некоторые вакцины содержат живые, ослабленные микроорганизмы. Многие из этих активных вирусов были культивированы в условиях, которые отключают их вирулентные свойства, или используют близкородственные, но менее опасные организмы для получения широкого иммунного ответа. Хотя большинство ослабленных вакцин являются вирусными, некоторые из них являются бактериальными по своей природе. Примеры включают вирусные заболевания желтая лихорадка, корь, паротит и краснуха , а также бактериальные заболевания брюшной тиф . Живая вакцина против туберкулеза микобактерий, разработанная фирмами Calmette и Guérin, не является заразной штамм but содержит вирулентно модифицированный штамм под названием "BCG", используемый для получения иммунного ответа на вакцину. Живая аттенуированная вакцина, содержащая штамм Yersinia pestis EV, используется для иммунизации чумой. Аттенуированные вакцины имеют некоторые преимущества и недостатки. Они обычно провоцируют более длительные иммунологические реакции и являются предпочтительным типом для здоровых взрослых. Но они могут быть небезопасны для использования у иммунокомпрометированных лиц и в редких случаях мутировать в вирулентную форму и вызывать заболевание.
Анатоксин[править]
Основная статья: Анатоксин
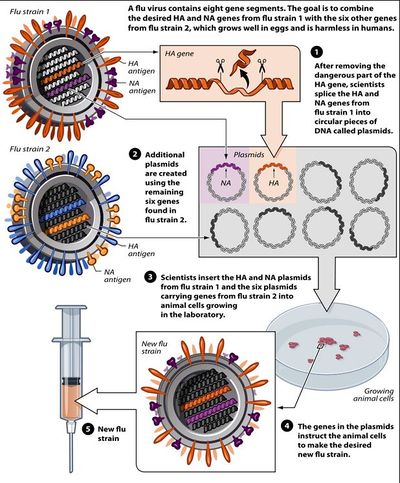
Анатоксиновые вакцины изготавливаются из инактивированных токсичных соединений, которые вызывают заболевание, а не микроорганизм. примерами вакцин на основе анатоксина являются вакцины против столбняка и дифтерии . Анатоксиновые вакцины известны своей эффективностью. не все анатоксины предназначены для микроорганизмов; например, анатоксин Crotalus atrox используется для вакцинации собак от укусов гремучих змей.
Подразделение[править]
Белковая субъединица - вместо того, чтобы вводить инактивированный или ослабленный микроорганизм в иммунную систему (которая будет представлять собой "цельноагентную" вакцину), ее фрагмент может создать иммунный ответ. Примеры включают субъединицу вакцины против вируса гепатита В, которая состоит только из поверхностных белков вируса (ранее выделенных из сыворотки крови хронически инфицированных пациентов, но теперь полученных рекомбинацией вирусных генов в дрожжи ) или в качестве съедобной водорослевой вакцины, вирусоподобной частицы (VLP) вакцины против вируса папилломы человека (ВПЧ), который состоит из вирусного основного капсидного белка [40] и субъединиц гемагглютинина и нейраминидазы вируса гриппа. субъединичная вакцина используется для иммунизации против чумы.
Спрягать[править]
Основная статья: Конъюгированная вакцина
Некоторые бактерии имеют полисахаридные наружные оболочки, которые плохо иммуногенны . Связывая эти внешние оболочки с белками (например, токсинами), иммунная система может быть приведена к распознаванию полисахарида, как если бы это был белковый антиген. Этот подход используется в вакцине против Гемофильного гриппа типа B.
Гетеротипный[править]
Основная статья: Гетерологичная вакцина
Также известные как гетерологичные или "Дженнеровские" вакцины, это вакцины, которые являются патогенами других животных, которые либо не вызывают заболевания, либо вызывают легкое заболевание в обрабатываемом организме. Классическим примером является использование Дженнером коровьей оспы для защиты от оспы. Одним из современных примеров является использование вакцины БЦЖ из микобактерий bovis для защиты от туберкулеза человека.
Экспериментальный[править]
Также разрабатывается и используется ряд инновационных вакцин:
- Вакцины против дендритных клеток объединяют дендритные клетки с антигенами, чтобы представить антигены к белым кровяным клеткам организма, тем самым стимулируя иммунную реакцию. Эти вакцины показали некоторые положительные предварительные результаты для лечения опухолей головного мозга [44], а также протестированы при злокачественной меланоме.
- Вакцинация ДНК - альтернативный, экспериментальный подход к вакцинации, называемый вакцинацией ДНК, созданный из ДНК инфекционного агента, находится в стадии разработки. Предлагаемый механизм заключается во внедрении (и экспрессии , усиленной с помощью электропорации , запускающей распознавание иммунной системы) вирусной или бактериальной ДНК в клетки человека или животных. Некоторые клетки иммунной системы, которые распознают экспрессируемые белки, будут атаковать эти белки и клетки, их экспрессирующие. Потому что эти клетки живут очень долго, если возбудитель то, что обычно экспрессируют эти белки, встречается в более позднее время, они будут атакованы мгновенно иммунной системой. Одним из потенциальных преимуществ ДНК-вакцин является то, что они очень просты в производстве и хранении. По состоянию на 2015 год вакцинация ДНК все еще является экспериментальной и не одобрена для использования человеком.
- Рекомбинантный вектор-сочетая физиологию одного микроорганизма и ДНК другого, можно создать иммунитет против заболеваний, имеющих сложные инфекционные процессы. Примером может служить вакцина RVSV-ZEBOV, лицензированная для Merck, которая используется в 2018 году для борьбы с Эболой в Конго .
- РНК-вакцина представляет собой новый тип вакцины, которая состоит из РНК нуклеиновой кислоты, упакованной в вектор, такой как липидные наночастицы. В настоящее время разрабатывается ряд РНК-вакцин для борьбы с пандемией COVID-19 .
- Т-клеточные рецепторные пептидные вакцины находятся в стадии разработки для нескольких заболеваний с использованием моделей долинной лихорадки, стоматита и атопического дерматита . Было показано, что эти пептиды модулируют выработку цитокинов и улучшают клеточный иммунитет.
- Таргетирование идентифицированных бактериальных белков, участвующих в ингибировании комплемента, нейтрализует ключевой механизм бактериальной вирулентности.
В то время как большинство вакцин создаются с использованием инактивированных или ослабленных соединений из микроорганизмов, синтетические вакцины состоят главным образом или полностью из синтетических пептидов, углеводов или антигенов.
Валентный[править]
Вакцины могут быть моновалентными (также называемые одновалентными ) или многовалентными (также называемые поливалентными ). Моновалентная вакцина предназначена для иммунизации против одного антигена или одного микроорганизма. многовалентная или поливалентная вакцина предназначена для иммунизации против двух или более штаммов одного и того же микроорганизма или против двух или более микроорганизмов.Валентность многовалентной вакцины может быть обозначена греческим или латинским префиксом (например, четырехвалентный или квадривалентный). В некоторых случаях моновалентная вакцина может быть предпочтительной для быстрого развития сильного иммунного ответа.
Номенклатура[править]
Были разработаны различные довольно стандартизированные сокращения для названий вакцин, хотя стандартизация никоим образом не является централизованной или глобальной. Например, названия вакцин, используемых в Соединенных Штатах, имеют хорошо известные сокращения, которые также широко известны и используются в других странах. Обширный список из них, представленный в сортируемой таблице и свободно доступный, доступен на веб-странице центров США по контролю и профилактике заболеваний. на странице поясняется ,что " сокращения [в] этой таблице (колонка 3) были стандартизированы совместно сотрудниками центров по контролю и профилактике заболеваний, ACIP Рабочие группы, редактор еженедельного отчета о заболеваемости и смертности (MMWR), редактор эпидемиологии и профилактики заболеваний, предупреждаемых вакцинами (розовая книга), члены ACIP и организации связи с ACIP." некоторыми примерами являются" Дтап "для дифтерийных и столбнячных анатоксинов и бесклеточной коклюшной вакцины," ДТ "для дифтерийных и столбнячных анатоксинов и" тд " для столбнячных и дифтерийных анатоксинов. На своей странице о вакцинации против столбняка, далее КДК поясняет ,что " прописные буквы в этих сокращениях обозначают полные дозы дифтерийных (D) и столбнячных (T) анатоксинов и коклюшной (P) вакцины. Строчные буквы "d" и " p " означают уменьшенные дозы дифтерии и коклюша, используемые в препаратах для подростков/взрослых. "А" в DTaP и Tdap означает "ацеллюлярный", что означает, что коклюшный компонент содержит только часть коклюшного организма." Еще один список установленных сокращений вакцин находится на странице CDC под названием" акронимы и сокращения вакцин", причем аббревиатуры используются в американских регистрах иммунизации. Принятая в США система наименований имеет некоторые условные обозначения для порядка слов названий вакцин, устанавливая головные существительные первыми и прилагательные постпозитивно . Вот почему USAN для " OPV "- это "полиовирусная вакцина живая оральная", а не"оральная полиовирусная вакцина".
Развитие иммунитета[править]
Иммунная система распознает вакцинные агенты как чужеродные, уничтожает их и "запоминает". Когда обнаруживается вирулентная версия агента, организм распознает белковую оболочку вируса и таким образом готовится к ответу, (1) нейтрализуя целевой агент, прежде чем он сможет войти в клетки, и (2) распознавая и уничтожая инфицированные клетки, прежде чем этот агент сможет размножиться до огромных чисел.
Когда две или более вакцины смешиваются вместе в одной и той же рецептуре, две вакцины могут вмешиваться. Это чаще всего происходит с живыми аттенуированными вакцинами, где один из компонентов вакцины более прочен, чем другие, и подавляет рост и иммунный ответ на другие компоненты. Это явление впервые было отмечено в трехвалентной вакцине против полиомиелита Сабина, где количество вируса серотипа 2 в вакцине должно было быть уменьшено, чтобы остановить его от вмешательства в "взятие" вирусов серотипа 1 и 3 в вакцине.[54] было обнаружено, что это явление также является проблемой с вакцины против денге в настоящее время исследуются, ] где было обнаружено, что серотип DEN-3 преобладает и подавляет ответ на серотипы DEN-1, -2 и -4.
Адъюванты и консерванты[править]
Вакцины обычно содержат один или несколько адъювантов, используемых для усиления иммунного ответа. Столбнячный анатоксин, например, обычно адсорбируется на квасцах . Это представляет антиген таким образом, чтобы произвести большее действие, чем простой водный столбнячный анатоксин. Люди, у которых есть неблагоприятная реакция на адсорбированный столбнячный анатоксин, могут получить простую вакцину, когда придет время для бустера.
В ходе подготовки к кампании 1990 года в Персидском заливе в качестве адъюванта против сибирской язвы использовалась цельноклеточная коклюшная вакцина. Это дает более быстрый иммунный ответ, чем предоставление только вакцины против сибирской язвы, что имеет некоторое преимущество, если воздействие может быть неизбежным.
Вакцины могут также содержать консерванты для предотвращения загрязнения бактериями или грибками . До недавнего времени консервант тиомерсал использовался во многих вакцинах, которые не содержали живого вируса. По состоянию на 2005 год, единственной детской вакциной в США, которая содержит тиомерсал в большем, чем следовые количества, количестве является вакцина против гриппа, которая в настоящее время рекомендуется только для детей с определенными факторами риска. Разовые вакцины против гриппа, поставляемые в Великобританию, не содержат тиомерсала в своих ингредиентах. Консерванты могут использоваться на различных стадиях производства вакцин, и самые сложные методы измерения могут обнаружить их следы в готовом продукте, как они могут быть обнаружены в окружающей среде и популяции в целом.
Расписание[править]
Основная статья: График вакцинации Для получения конкретной страновой информации о политике и практике вакцинации см. раздел Политика вакцинации .
В целях обеспечения наилучшей защиты детям рекомендуется делать прививки, как только их иммунная система будет достаточно развита, чтобы реагировать на конкретные вакцины, причем для достижения "полного иммунитета" часто требуются дополнительные "бустерные"прививки. Это привело к разработке комплексных графиков вакцинации. В Соединенных Штатах Консультативный комитет по практике иммунизации, который рекомендует дополнения графика для Центров по контролю и профилактике заболеваний, рекомендует плановую вакцинацию детей против: гепатита А, гепатита В, полиомиелита, паротита, кори, краснухи, дифтерия , коклюш , столбняк , HiB, ветряная оспа , ротавирус , грипп, менингококковая болезнь и пневмония . большое количество рекомендованных вакцин и бустеров (до 24 инъекций к двум годам) привело к проблемам с достижением полного соответствия. В целях борьбы со снижением показателей соблюдения были созданы различные системы уведомления, и в настоящее время на рынок поступает ряд комбинированных инъекций (например, пневмококковая конъюгированная вакцина и вакцина MMRV), которые обеспечивают защиту от многочисленных заболеваний.
Помимо рекомендаций по вакцинации младенцев и бустеров, многие конкретные вакцины рекомендуются для других возрастов или для повторных инъекций в течение всей жизни—чаще всего для кори, столбняка, гриппа и пневмонии. Беременные женщины часто проходят скрининг на постоянную устойчивость к краснухе. Вакцина против вируса папилломы человека рекомендуется в США (по состоянию на 2011 год) и Великобритании (по состоянию на 2009 год). рекомендации по вакцинации для пожилых людей сосредоточены на пневмонии и гриппе, которые являются более смертоносными для этой группы. В 2006 году была введена вакцина против опоясывающего лишая, заболевание, вызванное вирусом ветрянки, который обычно поражает пожилых людей.
История[править]
До введения вакцинации с использованием материала из случаев коровьей оспы (гетеротипическая иммунизация) оспу можно было предотвратить путем преднамеренной прививки вируса оспы, который впоследствии был назван вариоляцией, чтобы отличить его от вакцинации против оспы . Самые ранние намеки на практику прививки от оспы в Китае приходят в течение 10-го века.Китайцы также практиковали древнейшее документально подтвержденное использование вариоляции, восходящее к пятнадцатому веку. Они реализовали метод " назальной инсуффляции"вводится путем вдувания порошкообразного оспенного материала, обычно струпьев, в ноздри. На протяжении шестнадцатого и семнадцатого веков в Китае были зарегистрированы различные методы инсуффляции. Два доклада о китайской практике прививки были получены Королевским обществом в Лондоне в 1700 году; один-доктором Мартином Листером, который получил доклад сотрудника Ост-Индской компании, дислоцированной в Китае, а другой-Клоптоном Хейверсом
Где-то в конце 1760-х годов во время своего ученичества в качестве хирурга/аптекаря Эдвард Дженнер узнал историю, распространенную в сельских районах, что молочные рабочие никогда не будут иметь часто смертельную или уродующую болезнь оспу , потому что они уже заразились коровьей оспой , которая имеет очень мягкий эффект у людей. В 1796 году Дженнер взял гной из руки молочницы с коровьей оспой, нацарапал его на руке 8-летнего мальчика Джеймса Фипса, а через шесть недель привил ( вариолировал ) мальчика с оспой , впоследствии заметив, что он не заразился оспой. Дженнер продолжил свои исследования и в 1798 году сообщил, что его вакцина была безопасна для детей и взрослых и могла передаваться из рук в руки, уменьшая зависимость от неопределенных поставок от зараженных коров.Так как вакцинация коровьей оспой была намного безопаснее прививки оспы малой , последняя, хотя все еще широко практикуемая в Англии, была запрещена в 1840 году.
Второе поколение вакцин было введено в 1880-х годах Луи Пастером, который разработал вакцины против куриной холеры и сибирской язвы [11], а с конца XIX века вакцины считались вопросом национального престижа, и были приняты законы об обязательной вакцинации.
В XX веке было введено несколько успешных вакцин, в том числе против дифтерии , кори , паротита и краснухи . Основные достижения включали разработку вакцины против полиомиелита в 1950-х годах и искоренение оспы в 1960-х и 1970-х гг. Морис Хиллман был самым плодовитым из разработчиков вакцин в ХХ веке. По мере того как вакцины становились все более распространенными, многие люди стали воспринимать их как нечто само собой разумеющееся. Однако вакцины остаются неуловимыми для многих важных заболеваний , включая простой герпес , малярию , гонорею и ВИЧ .
Вакцины ликвидировали природную оспу и почти ликвидировали полиомиелит , в то время как другие заболевания , такие как тиф, ротавирус , гепатит А и В и другие , хорошо контролируются. Обычные вакцины охватывают небольшое число заболеваний, но не являются эффективными в борьбе со многими другими инфекциями.
Вакцины для всего организма[править]
Вакцины первого поколения - это вакцины всего организма-либо живые и ослабленные , либо убитые формы. живые аттенуированные вакцины, такие как вакцины против оспы и полиомиелита, способны индуцировать киллерные Т-клеточные (Т-C или CTL) реакции, хелперные Т-клеточные (Т-H ) реакции и иммунитет к антителам . Однако аттенуированные формы патогена могут превращаться в опасную форму и могут вызывать заболевания у иммунокомпенсированных реципиентов вакцины (например, больных СПИДом ). Хотя убитые вакцины не имеют такого риска, они не могут генерировать специфические киллерные Т-клеточные реакции и могут вообще не работать при некоторых заболеваниях.
Субъединичные вакцины[править]
Вакцины второго поколения были разработаны для снижения рисков, связанных с живыми вакцинами. Это субъединые вакцины, состоящие из специфических белковых антигенов (таких как столбнячный или дифтерийный анатоксин ) или рекомбинантных белковых компонентов (таких как поверхностный антиген гепатита В). Они могут генерировать Т-хелперы и антитела, но не киллерные Т-клеточные реакции.
ДНК-вакцина[править]
Основная статья: Вакцинация ДНК § история
ДНК-вакцины - это вакцины третьего поколения. Они содержат ДНК, которая кодирует определенные белки (антигены) от патогена. ДНК вводится в организм и поглощается клетками,чьи нормальные метаболические процессы синтезируют белки на основе генетического кода в плазмиде, которую они приняли. Поскольку эти белки содержат области аминокислотных последовательностей, характерных для бактерий или вирусов, они распознаются как чужеродные, и когда они обрабатываются клетками-хозяевами и отображаются на их поверхности, иммунная система предупреждается, что затем запускает иммунные реакции.
Кроме того, ДНК может быть инкапсулирована в белок для облегчения входа в клетку. Если этот капсидный белок включен в ДНК, то полученная вакцина может сочетать в себе потенциал живой вакцины без риска реверсии. В 1983 году Энцо Паолетти и Деннис Паникали из Департамента здравоохранения Нью-Йорка разработали стратегию производства рекомбинантных ДНК-вакцин с использованием генной инженерии для преобразования обычной вакцины против оспы в вакцины, которые могут быть способны предотвращать другие заболевания. они изменили ДНК вируса коровьей оспы путем вставки гена из других вирусов (а именно вируса простого герпеса, гепатита В и грипп).
В 2016 году в Национальном институте здравоохранения начались испытания ДНК-вакцины против вируса Зика . В исследовании планировалось принять участие до 120 человек в возрасте от 18 до 35 лет. Отдельно Inovio Pharmaceuticals и GeneOne Life Science начали испытания другой ДНК-вакцины против Зика в Майами. Вакцина NIH вводится в верхнюю часть руки под высоким давлением. Производство вакцин в больших объемах остается нерешенным.
В настоящее время проводятся клинические испытания ДНК-вакцин для профилактики ВИЧ.
Временная шкала[править]
Основная статья: Сроки введения вакцин
Экономика развития[править]
Одна из проблем в области разработки вакцин носит экономический характер: многие болезни, наиболее требующие вакцинации , включая ВИЧ, малярию и туберкулез, существуют главным образом в бедных странах. Фармацевтические фирмы и биотехнологические компании имеют мало стимулов для разработки вакцин против этих заболеваний, поскольку потенциал для получения дохода невелик. Даже в более богатых странах финансовые доходы обычно минимальны, а финансовые и другие риски велики.
Большинство разработок вакцин до настоящего времени опирались на "толчковое" финансирование со стороны правительства, университетов и некоммерческих организаций. многие вакцины были весьма экономически эффективными и полезными для общественного здравоохранения . число фактически вводимых вакцин резко возросло за последние десятилетия. такое увеличение, в частности количества различных вакцин, вводимых детям до поступления в школу, возможно, обусловлено правительственными мандатами и поддержкой, а не экономическими стимулами.
Патентное право[править]
Подача патентов на процессы разработки вакцин также может рассматриваться как препятствие для разработки новых вакцин. Из-за слабой защиты, обеспечиваемой патентом на конечный продукт, Защита инноваций в отношении вакцин часто осуществляется посредством патентования процессов, используемых при разработке новых вакцин, а также защиты секретности .
По данным Всемирной Организации Здравоохранения, самым большим препятствием для местного производства вакцин в менее развитых странах являются не патенты, а существенные финансовые, инфраструктурные и кадровые потребности, необходимые для выхода на рынок. Вакцины представляют собой сложные смеси биологических соединений, и, в отличие от лекарств, не существует истинных генерических вакцин. Вакцина, производимая на новом предприятии, должна пройти полное клиническое тестирование на безопасность и эффективность, аналогичные тем, которые были проведены на вакцине, производимой первоначальным производителем. Для большинства вакцин были запатентованы конкретные процессы. Их можно обойти с помощью альтернативных методов производства, но для этого требуется инфраструктура НИОКР и соответствующая квалифицированная рабочая сила. В случае нескольких относительно новых вакцин, таких как вакцина против вируса папилломы человека, патенты могут создать дополнительный барьер.
Производство[править]

Производство вакцины проходит в несколько этапов. Во-первых, генерируется сам антиген. Вирусы выращиваются либо на первичных клетках, таких как куриные яйца (например, при гриппе), либо на непрерывных клеточных линиях, таких как культивированные клетки человека (например, при гепатите А ). бактерии выращиваются в биореакторах (например, Haemophilus influenzae тип b). Кроме того, рекомбинантный белок, полученный из вирусов или бактерий, может быть получен в дрожжах, бактериях или клеточных культурах. После того, как антиген генерируется, он выделяется из клеток, используемых для его генерации. Вирус может нуждаться в инактивации, возможно, без необходимости дальнейшей очистки. Рекомбинантные белки нуждаются во многих операциях, включающих ультрафильтрацию и колоночную хроматографию. Наконец, вакцина разрабатывается путем добавления адъювантов, стабилизаторов и консервантов по мере необходимости. Адъювант усиливает иммунный ответ антигена, стабилизаторы увеличивают срок хранения, а консерванты позволяют использовать многодозные флаконы. комбинированные вакцины труднее разрабатывать и производить из-за потенциальной несовместимости и взаимодействия между антигенами и другими вовлеченными ингредиентами.
Развиваются технологии производства вакцин. Культивируемые клетки млекопитающих, как ожидается, будут становиться все более важными, по сравнению с обычными вариантами, такими как куриные яйца, из-за большей производительности и низкой частоты проблем с загрязнением. Технология рекомбинации, которая производит генетически детоксифицированную вакцину, как ожидается, будет расти в популярности для производства бактериальных вакцин, использующих анатоксины. Ожидается, что комбинированные вакцины уменьшат количество антигенов, которые они содержат, и тем самым уменьшат нежелательные взаимодействия, используя патоген-ассоциированные молекулярные паттерны .
В 2010 году Индия произвела 60 процентов мировой вакцины стоимостью около 900 миллионов долларов (670 миллионов евро).
Наполнители[править]
Помимо самой активной вакцины, в вакцинных препаратах присутствуют или могут присутствовать следующие вспомогательные вещества и остаточные производственные соединения:
- В качестве адъювантов добавляют соли алюминия или гели . Адъюванты добавляются для содействия более раннему, более мощному ответу и более стойкому иммунному ответу на вакцину; они позволяют снизить дозировку вакцины.
- Антибиотики добавляются к некоторым вакцинам для предотвращения роста бактерий во время производства и хранения вакцины.
- Яичный белок присутствует в вакцинах против гриппа и желтой лихорадки, поскольку они готовятся с использованием куриных яиц. Могут присутствовать и другие белки.
- Формальдегид использован для того чтобы деактивировать бактериальные продукты для вакцин анатоксина. Формальдегид также используется для инактивации нежелательных вирусов и уничтожения бактерий, которые могут загрязнять вакцину во время производства.
- Глутамат натрия (MSG) и 2 - феноксиэтанол используются в качестве стабилизаторов в нескольких вакцинах, чтобы помочь вакцине оставаться неизменной, когда вакцина подвергается воздействию тепла, света, кислотности или влажности.
- Тиомерсал-это ртутьсодержащий антимикробный препарат, который добавляют во флаконы вакцины, содержащие более одной дозы, чтобы предотвратить загрязнение и рост потенциально вредных бактерий. Из-за разногласий, связанных с тиомерсалом, он был удален из большинства вакцин, за исключением многоцелевого использования гриппа, где он был снижен до уровней, так что одна доза содержала менее 1 микрограмма ртути, уровень, аналогичный употреблению 10 г консервированного тунца.
Роль консервантов[править]
Многие вакцины нуждаются в консервантах для предотвращения серьезных побочных эффектов, таких как стафилококковая инфекция, которая в одном случае 1928 года убила 12 из 21 ребенка, привитых дифтерийной вакциной, в которой не было консерванта.[95] несколько предохранителей доступны, включая тиомерсал, феноксиэтанол , и формальдегид . Тиомерсал более эффективен против бактерий, имеет более лучший срок годности при хранении, и улучшает вакцинную стабильность, мощь, и безопасность; но, в США, Европейский Союз и в некоторых других богатых странах он больше не используется в качестве консерванта в детских вакцинах, в качестве меры предосторожности из-за его содержания ртути.[96] хотя были выдвинуты противоречивые утверждения о том , что тиомерсал способствует развитию аутизма, никакие убедительные научные доказательства не подтверждают эти утверждения. кроме того, 10-11-летнее исследование 657 461 ребенка показало, что вакцина MMR не вызывает аутизм и фактически снижает риск развития аутизма на 7 процентов.
Средства доставки[править]

Разработка новых систем доставки повышает надежду на то, что вакцины будут безопаснее и эффективнее доставляться и применяться. Направления исследований включают липосомы и ISCOM (иммуностимулирующий комплекс).[100]
К числу заметных достижений в области технологий доставки вакцин относятся оральные вакцины. Ранние попытки применения оральных вакцин показали различную степень перспективности, начиная с начала 20-го века, в то время как сама возможность эффективной оральной антибактериальной вакцины была спорной. к 1930-м годам возрос интерес к профилактической ценности оральной вакцины против брюшного тифа, например.
Оральная вакцина против полиомиелита оказалась эффективной, когда прививки делались добровольцами без формальной подготовки; результаты также продемонстрировали возросшую легкость и эффективность введения вакцин. Эффективные пероральные вакцины имеют много преимуществ; например, отсутствует риск заражения крови. Вакцины, предназначенные для перорального введения, не обязательно должны быть жидкими, а в качестве твердых веществ они обычно более стабильны и менее подвержены повреждению или порче путем замораживания при транспортировке и хранении.[103] такая стабильность уменьшает потребность в " холодной цепи": ресурсы, необходимые для поддержания вакцин в ограниченном температурном диапазоне от стадии изготовления до момента введения, что, в свою очередь, может привести к снижению затрат на вакцины.
Микроигольный подход, который все еще находится на стадии разработки, использует "заостренные проекции, изготовленные в массивы, которые могут создавать пути доставки вакцины через кожу".
Экспериментальная система доставки вакцины без иглы проходит испытания на животных. пластырь размером с Марку, похожий на клейкую повязку, содержит около 20 000 микроскопических выступов на квадратный сантиметр.[108] это кожное введение потенциально повышает эффективность вакцинации, требуя при этом меньше вакцины, чем инъекции.
Плазмиды[править]
Использование плазмид было подтверждено в доклинических исследованиях в качестве защитной вакцинной стратегии против рака и инфекционных заболеваний. Однако в исследованиях на людях этот подход не принес клинически значимых результатов. Общая эффективность иммунизации плазмидной ДНК зависит от повышения иммуногенности плазмиды при одновременной коррекции факторов, участвующих в специфической активации клеток-эффекторов иммунитета.
Ветеринарная медицина[править]
Смотрите также: Вакцина против гриппа § Вакцина против гриппа для негуманоидов и вакцинация собак

Прививки животных используются как для предотвращения их заражения болезнями, так и для предотвращения передачи болезни людям. как домашние животные, так и животные, выращенные в качестве домашнего скота, регулярно вакцинируются. В некоторых случаях дикие популяции могут быть привиты. Это иногда достигается при распространении зараженной вакцинами пищи в подверженных заболеваниям районах и используется для борьбы с бешенством енотов .
В тех случаях, когда возникает бешенство, вакцинация собак от бешенства может потребоваться по закону. Другие собачьи вакцины включают чумку собак , парвовирус собак , инфекционный собачий гепатит , аденовирус-2 , лептоспироз , бордателлу , вирус парагриппа собак и болезнь Лайма , среди других.
Были задокументированы случаи использования ветеринарных вакцин у людей, будь то преднамеренные или случайные, с некоторыми случаями возникновения в результате этого заболевания, особенно с бруцеллезом . однако сообщения о таких случаях встречаются редко, и очень мало было изучено о безопасности и результатах такой практики. С появлением аэрозольной вакцинации в ветеринарных клиниках для животных-компаньонов в последние годы, вероятно , возросло воздействие на человека патогенов, которые не переносятся естественным путем в организме человека, таких как Bordetella bronchiseptica. в некоторых случаях, особенно при бешенстве параллельная ветеринарная вакцина против патогена может быть на несколько порядков более экономичной, чем человеческая.
Вакцины от дивы[править]
DIVA (дифференциация инфицированных от вакцинированных животных), также известная как SIVA (сегрегация инфицированных от вакцинированных животных), вакцины позволяют дифференцировать инфицированных и вакцинированных животных.
Вакцины DIVA несут по крайней мере на один эпитоп меньше, чем микроорганизмы, циркулирующие в полевых условиях. Сопутствующий диагностический тест, который обнаруживает антитела против этого эпитопа, позволяет нам фактически сделать эту дифференцировку.
Первые вакцины дивы[править]
Первые вакцины DIVA (ранее называвшиеся маркерными вакцинами и с 1999 года придуманные как вакцины DIVA) и сопутствующие диагностические тесты были разработаны компанией J. T. van Oirschot и коллеги из Центрального ветеринарного института в Лелистаде, Нидерланды. Они обнаружили, что некоторые существующие вакцины против псевдорабий (также называемая болезнью Ауески) имела делеции в их вирусном геноме (среди которых был ген gE). Моноклональные антитела были получены против этой делеции и отобраны для разработки ИФА, который продемонстрировал антитела против gE. Кроме того, были созданы новые генно-инженерные gE-отрицательные вакцины. Кроме того, были разработаны вакцины DIVA и сопутствующие диагностические тесты против герпесвирусной инфекции крупного рогатого скота 1.
Использовать на практике[править]
Стратегия DIVA была применена в различных странах и успешно ликвидировала вирус псевдорабии. Популяции свиней интенсивно вакцинировались и контролировались с помощью сопутствующего диагностического теста, а затем зараженные свиньи были удалены из популяции. Вакцины против бычьего герпеса 1 DIVA также широко используются на практике.
Другие вакцины против дивы (в стадии разработки)[править]
Ученые приложили и до сих пор прилагают много усилий в применении принципа DIVA к широкому спектру инфекционных заболеваний, таких как, например, классическая лихорадка свиней, птичий грипп, Актинобактериальная плеуропневмония и сальмонеллезные инфекции у свиней.
Тренды[править]
Тенденции
Разработка вакцины имеет несколько тенденций:
- До недавнего времени, большинство вакцин были направлены на младенцев и детей, но подростки и взрослые все чаще становятся мишенью.
- Комбинации вакцин становятся все более распространенными; вакцины, содержащие пять или более компонентов, используются во многих частях мира.
- Разрабатываются новые методы введения вакцин, ] как заплаты кожи, аэрозоли через приборы вдыхания, и еда genetically проектированных заводов.
- Вакцины разрабатываются для стимулирования врожденных иммунных реакций, а также для адаптации.
- Предпринимаются попытки разработать вакцины для лечения хронических инфекций, а не для профилактики заболеваний.
- Разрабатываются вакцины для защиты от биотеррористических нападений, таких как сибирская язва, чума и оспа.
- Признание различий в отношении пола и беременности в ответах на вакцины "может изменить стратегии, используемые должностными лицами в области общественного здравоохранения".[123]
- Ученые сейчас пытаются разработать синтетические вакцины, реконструируя внешнюю структуру вируса, это поможет предотвратить резистентность вакцины.
Принципы, которые управляют иммунным ответом, теперь могут быть использованы в индивидуальных вакцинах против многих неинфекционных заболеваний человека, таких как рак и аутоиммунные расстройства. например, экспериментальная вакцина CYT006-AngQb была исследована как возможное лечение высокого кровяного давления . факторы, влияющие на тенденции развития вакцин , включают прогресс в области трансляционной медицины , демографии, регулятивной науки, политических, культурных и социальных ответных мер.
Установки-биореакторы для производства вакцин[править]
Трансгенные растения были определены как перспективные экспрессионные системы для производства вакцин. Сложные растения, такие как табак, картофель, помидор и банан, могут иметь гены, которые заставляют их производить вакцины, пригодные для использования людьми.[128] были разработаны бананы, которые производят человеческую вакцину против гепатита В.[129] Другим примером является экспрессия белка слияния в трансгенных растениях люцерны для селективного направления к антигенпрезентирующим клеткам, что повышает эффективность вакцины против вируса вирусной диареи крупного рогатого скота (BVDV).
Смотреть также[править]
- Охладитель вакцины
- Коалиция по обеспечению готовности к эпидемиям инновации
- Экономика вакцин
- Летучий шприц
- Лошадь По Кличке Джим
- Регистр иммунизации
- Иммунотерапия
- Список компонентов вакцины
- Перечень тем для вакцинации
- Неспецифическое действие вакцин
- OPV СПИД гипотеза
- Обратная Вакцинология
- ТА-КД
- Виросом
- Провал вакцины
- Вакцинная нерешительность
- Вакцинов
- Вирусоподобная частица